本文描述了與生物藥物產品的凍干相關的挑戰。采用質量源于設計(QbD)方法和SP Line of Sight™技術套件, 提供了一個豐富的數據環境,其中許多挑戰可以被克服。Line of Sight™包含全套的設備、技術和PAT工具,可以簡化凍干制劑從早期開發到生產放大,加速商業化生產。從事于生物制劑的公司需要靠得住的流程和經過驗證的數據來交付成功的產品。

生物藥物在治療許多改變生活的疾病方面顯示出了巨大的前景,甚至包括一些曾經被認為無法治愈的疾病。然而,由于生物材料的敏感性,它需要專門的開發和制造工藝。凍干的穩定性對保持產品的生物活性、結構完整性和質量均一性是非常有吸引力的,而所有這些都是產品成功的關鍵。
1、背景介紹
臨床管線中50%的藥物由生物制劑組成。大的生物分子,通常是蛋白質或抗體,給藥需要不同于標準固體或半固體藥物制劑的制造能力。生物藥物和抗體-偶聯藥物(ADCs)不僅生產成本很高,而且有些還不如其他制劑或分子穩定。在儲存和運輸過程中保存它們的活性也是非常困難的。此外,產品溫度監測的重要性不能低估,特別是當工藝轉移到具有無菌環境的較大設備時,應將測量產品溫度的解決方案視為開發策略的一部分。
為了克服這些要求并延長保質期,冷凍干燥是相對較好的方式。凍干過程將產品的溫度降低到冰點以下,然后使用受控真空升華除去水或其他溶劑。至少41%的生物藥品和幾乎所有ADCs都是冷凍干燥的,以保持其物理結構。ADCs的凍干可保障在儲存和運輸過程中連接“ payload”與antibody的 linker的穩定性。凍干生物制劑可以快速復水,同時保持其生物活性。
冷凍干燥過程中的每一部分都對產品的質量和完整性有很大的影響。隨著技術的進步和更多工具的運用,人們可以更好地理解如何測量和記錄影響最終產品的參數,從而對產品本身有更多的了解。美國FDA和其他監管機構強烈建議采用質量設計(QbD)方法,以確保產品性能。FDA早在2011年1月發布的過程驗證指南中指出:“企業需要繼續從獲得的知識中受益,并通過調整在整個過程生命周期中不斷改進,使得生產問題的根源迅速得到糾正”。這種從試錯方法到基于科學的凍干過程方法的轉變,為這些生物藥物的體內產品性能提供了信心。
2、QbD方法—優化凍干生物制劑
生物藥物數量的增加往往服務于小目標人群,這導致對開發人員和制造商的更大要求,以提高產量和更好的產品質量來提高效率。批次內部和批次之間的一致性是基于從物理外觀和結構完整性到生物活性等幾個特性的整體質量參數。注射用藥物在生產過程中也要求高度無菌。在無菌環境中,通過加強對冷凍干燥過程的控制,可以縮短開發時間,提高穩定性和質量。
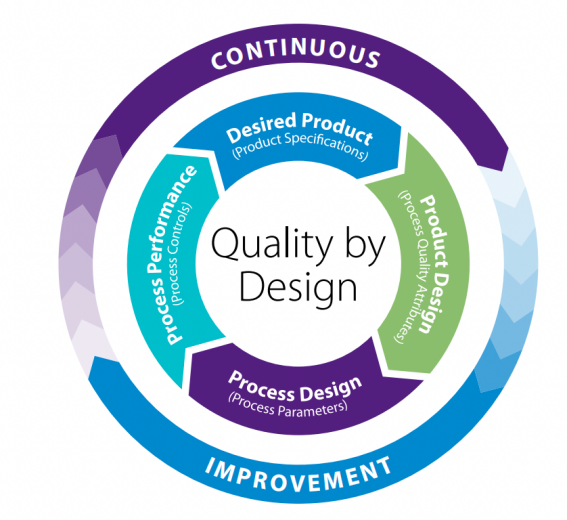
圖1:質量源于設計(QbD)方法
要解決這些挑戰,首先要在產品生命周期的早期對其有一個很好的理解。從一開始就更好地開發冷凍干燥工藝以實現較理想的的大規模商業化,并從長遠來看降低經濟負擔。然而,即使有了這些知識,擴大規模對生物藥物制造商來說仍然是一個持續的挑戰。凍干設備的性能和操作在開發和生產規模之間可能存在差異,這導致在每個階段對凍干參數進行耗時和昂貴的重新優化,以實現產品的成功凍干。
藥品生產QbD方法的一部分是利用過程分析技術(PAT)改進冷凍干燥工藝,以便能夠很好地定義關鍵工藝參數,并及時了解和監測其對產品質量的影響。要特別注意這些參數將創造一個優化的設計操作空間,從而降低成本。
3、理解設計空間
作為QbD方法的一部分,一種系統的開發方法從預定義的目標開始應用,并強調對產品和過程的理解。這得到了科學知識和質量風險管理的支持,以建立一個設計空間和已定義的操作變量集,以保持批處理的一致性(圖2)。這些參數以圖形方式表示為多維點,以定義維護批處理一致性所需的操作變量集。 在設計空間(操作空間)內的操作將使產品達到預定義的質量。
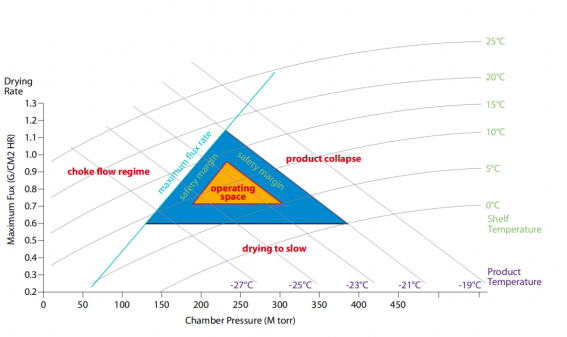
圖2:凍干工藝的設計空間
設計空間的簡化描述——設備能力極限和產品知識的多維表示
4、一套工具—用于生物制藥凍干生產放大
Line of Sight™

認識到生產放大的內在挑戰和對改善生物藥物開發和制造結果的愿望,ATS SP創建了Line of Sight (LoS)。
LoS是一套工具——技術和設備,可用于開發和生產的每個階段,以提高凍干過程控制、效率、質量和一致性。
這套技術和PAT被內置到小型冷凍干燥機中,通過大型商業化生產凍干機為研究和生產凍干專業人員提供了一種清晰的,由實時數據支持的流程方法。這種方法還使得一種設備的技術和方法可以復制并直接與另一種設備進行比較。
LoS的工具包括:
● Lyoccapsule™微型冷凍干燥機:7瓶開發-適用于昂貴的藥物和早期配方或工藝開發;
● LyoStar™4.0研發型冷凍干燥機:凍干工藝開發和優化的“主力”及”優選工具“;
● LyoConstellation™系列大型冷凍干燥機:不僅可以進行凍干工藝開發,還可以提供無菌GMP操作。
所有這些凍干機都配備PAT工具,包括:
● ControLyo®技術用于晶核控制 ;
● SMART™技術用于加速初級干燥開發和優化;
● LyoFlux* TDLAS蒸汽質量流量傳感器,非侵入式實時監測關鍵產品和過程數據;
● 無線Tempris*傳感器用于產品溫度測量;
5、提高凍干工藝效率
凍干效率依賴于獲得具有較少浪費(材料、能量、時間、金錢)的高質量產品。創建設計空間的預定義的操作變量集決定了過程效率。擁有更大的設計空間,或要工作的參數,可以增加重復執行成功工藝的概率,即使面對潛在的問題,包括計劃外的過程偏差。LoS可以通過理解流程參數如何影響關鍵的產品屬性來擴展特定目標的設計空間。
6、一次干燥工藝優化工具
SMART冷凍干燥技術
SMART冷凍干燥技術是一項PAT工具,使用壓力溫度測量(MTM)技術來確定凍干餅的阻力和升華界面的產品溫度。隨著AutoMTM允許研究人員在報告關鍵工藝和產品參數時運行自己的預定周期。SMART技術已被證明可以節省大量寶貴的開發時間,并提供過程相關的關鍵產品數據。
在與一家大型制藥公司和兩家生物技術公司的比較研究中,SMART技術被用于開發對應配方的優化周期。所有三個實驗室報告表明,他們在不到三個月的時間內收回了投資,平均開發時間縮短了62天。此外,科學家通常能夠在單次實驗運行后產生一個優化的工藝,這樣就有時間進行進一步的實驗來測試工藝極限。這些結果還意味著,一種配方可以比目前的時間框架提前幾個月進入中試生產階段。
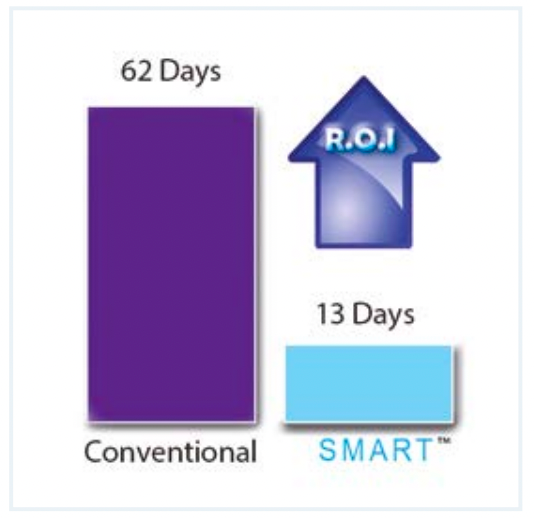
圖3:投資回報(ROI)示例:使用傳統方法VS Smart 技術開發工藝
7、準確測量蒸汽質量流量
PAT工具——TDLAS
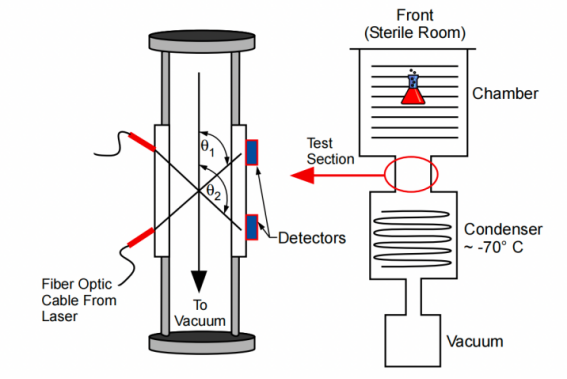
圖4:應用于Lyostar 凍干機上的TDLAS技術
通過LoS技術套件中的另一個PAT工具(TDLAS)可以對凍干過程和放大進行有效實時監測和測量。LyoFlux傳感器使用可調諧二極管激光吸收光譜(TDLAS)技術來測量水蒸氣濃度和流速,由此可以得出特定配方的升華界面溫度。LyoFlux可以在短短三個實驗中計算特定產品的工藝設計空間參數,而傳統上至少需要5次或6次運行。使用LyoFlux技術,可以通過一次運行獲得最大升華速率來確定設備性能。一旦該設備的設備能力建立,可以確定用于產品的小瓶的傳熱系數Kv。同樣,LyoFlux可以通過改變腔室壓力和監測各自壓力設定點的升華速率,在一次測試中執行多個實驗。LyoFlux還可以確定在小瓶中冷凍干燥過程中的餅阻力。這簡化了生產冷凍干燥機的使用,并盡可能大限度地減少了進行多組實驗所需的停機時間,從而獲得產品屬性和設備性能數據,以便進一步分析設計空間。
8、對冰成核的精確控制
ControLyo技術
過冷程度是冷凍干燥放大的一大挑戰。溫度越低,過冷的程度就越高,導致冰晶變小。這會影響升華率和產品溫度分布,導致實驗室生成周期和商業制造生成周期之間的性能差異。冷凍是一個隨機過程,凍干機內的小瓶在不同時間隨機發生成核,產生異質批次和藥品耐藥性的可變性。
ATS SP Scientific的ControLyo技術利用惰性氣體和一系列增壓和減壓步驟,實現在較高溫度下控制所有小瓶瞬時成核。這將極大限度地減少過冷,并產生盡可能大的冰晶。當冰升華時,大晶體產生更大的空腔,使內部區域后續干燥的阻力更小,潛在干燥時間短,最終產品更容易復水。研究表明,成核溫度每升高1℃,一次干燥時間減少3%。在某些情況下,ControLyo已被證明可以將周期時間從7.5縮短到5.5天,提高了生產率并提供了經濟效益。

圖5:ControLyo技術精確控制冰成核
許多新型生物藥物的配方復雜,蛋白質含量高,灌裝量大,在冷凍干燥時面臨著很大的挑戰。使用ControLyo可以確保較低的產品阻力,并提高批內與批間產品的均一性。因此,能為產品提供更積極的周期,擴大設計空間。ControLyo的另一個優點是,它可以安裝或改裝到任何冷凍干燥機上。
9、只需7個小瓶—加速凍干工藝開發
由于生物制劑的活性藥物成分(API)價格昂貴,可用于冷凍干燥開發和優化的數量有限。LoS技術套件內的冷凍干燥機包括一個微型凍干機Lyoccapsule(圖6),配備了創新的PAT工具和技術,且與SP其它更大規模的凍干機保持一致性。
Lyoccapsule只需7個小瓶,使用的材料更少,資源和準備時間也更少。這使得篩選更多的配方和優化干燥條件成為可能,遠比在大型冷凍干燥機中更好。大一點規模的研發型及中試放大型凍干機,如LyoStar 4.0或 LyoConstellation,有助于進一步的工藝開發、優化、實驗室規模的穩定性研究和放大。LyoConstellation凍干機的范圍可以進一步用于從幾百到幾千瓶的批次的全面商業化生產。

圖6:LyoCapsule: 7瓶微型研發型凍干機
10、從早期開發到商業化的平穩過渡
無論是在早期開發階段、臨床階段、中試批次還是商業化生產階段,有效生產高質量產品的關鍵參數都是相同的。然而,由于每個階段設備之間的差異,從一個階段轉移到另一個階段通常需要反復優化。
LoS技術套件由產品開發的每個階段(Lyoccapsule, LyoStar 3, LyoConstellation)的凍干機組成,旨在通過在每個凍干機中提供經過驗證的技術(SMART, LyoFlux TDLAS, Tempris和ControLyo)的連續性來盡可能大限度地減少這些差異。這種方法在每個階段對結果進行了有意義的比較。
一些生物技術和制藥公司已經認識到LoS對放大產品凍干過程的重要性。一家生物技術公司的一位科學家曾報告說:“Lyoccapsule可以用更少的API測試更多的條件,從而限制了財務風險。在產品開發的放大過程中使用相同的技術可以提供對產品更全面的理解,并且比傳統的試錯方法增加了成功的可能性。
11、結論
人類生長激素、胰島素和紅細胞刺激劑等生物制劑的開發,為新的治療方式和生物療法開辟了道路,這些藥物可以用于對抗許多以前無法治愈的疾病。隨著臨床階段的評估,許多分子的市場規模呈指數級增長。由于其復雜性和特點,生物制品的開發、制造和分銷面臨著許多挑戰。通過凍干來穩定藥物被認為是保持藥物產品的生物活性、結構完整性和均一性的理想方法。
SP Line of Sight™
在明確的設計空間內開發和制造的QbD方法被認為是理想的實踐之一,任何監管機構都期望采用。從對產品和條件的準確監測到整個冷凍干燥過程,ATS SP Line of Sight™工具套件支持QbD,以改進開發過程并保障生產的成功。LoS的設備設計和整合技術增加了操作空間的靈活性,提高了批量一致性,產量和產品質量。

圖5:SP Line of Sight (LoS)
此外,該行業對凍干工藝的關鍵工藝參數和產品質量的非侵入式測量越來越感興趣。這是由自動化的興起推動的,因為 FDA要求將人員從流程中移除,以保護產品免受操作人員的傷害,以及開發高效配方以保護操作人員免受產品的影響。
LoS的一系列冷凍干燥器和創新技術使凍干條件在產品開發的早期階段得到優化,提供產品知識,然后順利轉移到臨床和生產階段,而無需在每個階段進行昂貴的重新優化。通過靈敏和無菌的監測裝置和已建立的技術,可以準確、非侵入式地測量關鍵的凍干產品參數,提供一個豐富的數據環境。
這里的證據證明了優質生物藥品生產設施所能獲得的價值。通過投資ATS SP全套放大化技術,產品可以更有效地通過不同的開發階段走向商業化。這些技術為持續理解受過程變量影響的質量屬性提供了相同水平的產品和過程知識。這些努力簡化了開發過程并建立了一致的產品質量,以降低長期經濟負擔并支持更佳患者治療效果。

12、萊奧德創凍干課程
關注“萊奧德創凍干工場“,立即獲取凍干講堂的線上培訓課程。
基于對于凍干研發的一些考量,萊奧德創創建了金字塔凍干培訓平臺:包含了從凍干理論基礎,到配方和工藝開發,再到放大及生產,以及進階的設備管理和線上線下專題培訓課程
免責聲明
- 凡本網注明“來源:儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 移動端
移動端






 回放
回放
 回放
回放




















 浙公網安備 33010602002722號
浙公網安備 33010602002722號
2025廣州國際分析測試及實驗室設備展覽會暨技術研討會
展會城市:廣州市展會時間:2025-03-05